নিষ্ক্রিয় গ্যাস
নিষ্ক্রিয় গ্যাস বলতে পর্যায় সারণির ১৮তম শ্রেণীর[১] মৌলগুলোকে বোঝায়। কখনওবা একে অষ্টম শ্রেণী, হিলিয়াম পরিবার বা নিয়ন পরিবার নামে ডাকা হয়। ইংরেজিতে সচরাচর Gas হিসাবে অভিহিত। এই শ্রেণীতে অবস্থিত গ্যাসগুলো রাসায়নিকভাবে খুবই নিষ্ক্রিয়, কারণ এদের পরমাণুর সর্ববহিরস্থ কক্ষপথে ইলেকট্রনের সংখ্যা পরমাণুর সর্বোচ্চ ধারণ ক্ষমতার সমান অর্থাৎ ৮টি। ইতিমধ্যে সুস্থিত ইলেক্ট্রণসমূহ অন্য কোন মৌলের সাথে সহজে বিক্রিয়া করতে চায় না। সাধারণ অবস্থায় এগুলো বর্ণহীন, গন্ধহীন উচ্চ আয়নিক বিভব সম্পন্ন এবং এক পরমাণুক গ্যাস। উপরন্তু এগুলোর স্ফুটনাংক ও গলনাংক খুবই কাছাকাছি। আলোকসজ্জা, ওয়েল্ডিং এবং মহাশূন্য প্রযুক্তিতে এই গ্যাসগুলোর প্রভূত ব্যবহার রয়েছে। নিষ্ক্রিয় গ্যাসের সংখ্যা সাত। এগুলো হল: হিলিয়াম, নিয়ন, আর্গন, ক্রিপ্টন, জেনন, র্যাডন এবং ওগানেসন।[২]একে নোবেল গ্যাস বলা হয়
| নিষ্ক্রিয় গ্যাস | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||
আবিষ্কারের ইতিহাস
সম্পাদনানিষ্ক্রিয় গ্যাস মৌলসমূহের আবিষ্কার রসায়নের ইতিহাসে একটি বিশেষ উল্লেখযোগ্য ঘটনা। ১৭৮৫ খ্রিষ্টাব্দে বিজ্ঞানী ক্যাভেনডিস একটি আবদ্ধ পাত্রে কস্টিক সোডা দ্রবণের উপর অতিরিক্ত অক্সিজেনযুক্ত বায়ুতে বার বার বিদ্যুৎ স্ফুলিংগ প্রয়োগ করে অতি সামান্য পরিমাণ বায়ুর মূল আয়তনের প্রায় ১২০/১ ভাগ গ্যাসীয় অবশেষ পেলেন। তিনি পর্যবেক্ষণ করলেন যে, এই প্রক্রিয়ায় সমস্ত নাইট্রোজেনই অক্সাইডে পরিণত হয় এবং দ্রবণে অবশোষিত হয়ে সামান্য পরিমাণ গ্যাসীয় অবশেষ থাকে। তিনি আরও পর্যবেক্ষণ করলেন যে,এই অবিশষ্ট গ্যাস নাইট্রোজেন অপেক্ষাও নিষ্ক্রিয়। ক্যাভেনডিসের এই পরীক্ষার তাৎপর্য বিজ্ঞানীদের নিকট পরবর্তী প্রায় একশত বর্ষ উপেক্ষিত ছিল।
১৮৯৪ খ্রিষ্টাব্দে নাইট্রোজেন, অক্সিজেন প্রভৃতি বিভিন্ন গ্যাসীয় পদার্থের ঘনত্ব পরিমাপ করতে গিয়ে লর্ড রেলে (Lord Rayleigh) পর্যবেক্ষণ করেন যে, বিভিন্ন উৎস থেকে প্রাপ্ত অক্সিজেনের ঘনত্ব প্রতি ক্ষেত্রে অভিন্ন হলেও নাইট্রোজেনের ক্ষেত্রে ফলাফল ভিন্নরূপ। তিনি তিন পদ্ধতিতে নাইট্রোজেন আহরণ করলেন। যথাঃ (ক) অ্যামোনিয়াম নাইট্রাইটকে উত্তাপিত করে, (খ)নাইট্রোজেন অক্সাইডকে উত্তপ্ত লৌহ যোগে বিজারিত ক'রে ও (গ) সোডিয়াম হাইপোব্রোমাইটের ক্রিয়ায় ইউরিয়া থেকে নাইট্রোজেন সংগ্রহ করা। বিস্ময়ের সঙ্গে তিনি লক্ষ্য করলেন যে বায়ু হতে প্রাপ্ত নাইট্রোজেন রাসায়নিক উপায়ে প্রাপ্ত নাইট্রোজেন অপেক্ষা ভারী। এতে প্রতীয়মান হলো যে, বায়বীয় নাইট্রোজেনে নাইট্রোজেন ব্যতীত ভিন্ন কোন উপাদান রয়েছে। অতঃপর রেলে ক্যাভেনডিসের অনুরূপ পরীক্ষাকার্য চালিয়ে প্রাপ্ত গ্যাসীয় অবশেষে (residual gas) বর্ণালী বিশ্লেষণ ক'রে বায়ুতে বিদ্যমান, নাইট্রোজেন অপেক্ষা ভারী অথচ তদাবধি অনাবিষ্কৃত কোন গ্যাসের অস্তিত্ব কল্পনা করেন। পরে বিজ্ঞানী রেলে'এর অনুমতিক্রমে উইলিয়াম র্যামজি (Ramsay) গ্যাসীয় অবশেষটি পৃথক করতে চেষ্টা করেন। কার্বন ডাই-অক্সাইড ও জলীয় বাষ্পবিহীন বায়ু নিয়ে সেই বায়ু বার বার তপ্ত ম্যাগনেসিয়ামের ওপর দিয়ে প্রবাহিত করে নাইট্রোজেনকে ম্যাগনেসিয়াম নাইট্রাইড হিসেবে দ্রবীভূত করা হয়ঃ 3Mg +N2 = Mg3N2; এবং পরিলক্ষিত হয় যে, মূল আয়তনের ৮০/১ ভাগ গ্যাসীয় অবশেষে থেকে যায়। অথচ NO, N2O, NH4NO2 প্রভৃতি থেকে উৎসারিত নাইট্রোজেনকে ক্রমান্বয়ে উত্তপ্ত তামা ও ম্যাগনেসিয়ামের ওপর দিয়ে চালনা করে পরিলক্ষিত হয় যে, কোন গ্যাসীয় অবশেষ আদৌ থাকে না। রেলে ও উইলিয়াম র্যামজির প্রাপ্ত গ্যাসীয় অবশেষের বর্ণালি বিশ্লেষণে সম্পূর্ণ অজ্ঞাত সবুজ ও লাল রেখা বর্ণালীর সন্ধান লাভ করেন। পরিলক্ষিত হলো যে, এর ঘনত্ব ১৯.৯৪ (H-1), পারমাণবিক ভর ৪০ এবং এটি রাসায়নিক বিক্রিয়ায় এটি সম্পূর্ণ নিষ্ক্রিয় ভূমিকা পালন করে। এমনকী বিদ্যুৎ স্ফুলিঙ্গ প্রয়োগেও ক্লোরিন বা ফ্লোরিনের সাথে এর কোন রাসয়নিক বিক্রিয়া সংঘটিত হয় না। রেলে ও উইলিয়াম র্যামজি রাসায়নিক নিষ্ক্রিয়তার কারণে নতুন গ্যাস মৌলের নামাকরণ করেন আর্গন বা অলস। কিন্তু পরবর্তীকালে প্রমাণিত হয় যে, উক্ত গ্যাসীয় অবশেষটি বিশুদ্ধ আর্গন নয় এবং এতে আরও বিভিন্ন গ্যাস মৌল রয়েছে।
১৮৬৮ খ্রিষ্টাব্দের ১৮ই আগস্ট তারিখে ফরাসি জ্যোতির্বিদ জানসেন (Janssen) ভারতে দৃষ্ট পূর্ণ সূর্য গ্রহণের সময় গ্যাসীয় সৌর আবরণের মধ্যে বর্ণালী পর্যবেক্ষণ করে একটি স্পষ্ট পীত রেখা D3 আবিষ্কার করেন। এই রেখা সোডিয়ামের D1 ও D2 রেখা থেকে সম্পূর্ণ স্বতন্ত্র। পরে লকিয়ার (LocKyer) ও ফ্রাঙ্কল্যাণ্ড (Frankland) বিবিধ পরীক্ষা-নিরীক্ষার সাহায্যে এমত সিদ্ধান্তে উপনীত হন যে, যে উক্ত রেখা কোন অপার্থিব মৌলের সূচক—যা কেবল গ্যাসীয় সৌর আবরণেই বিদ্যমান। এ কারণে গ্রীক ‘হেলিওস’ (halios-সূর্য) শব্দানুক্রমে এর নামাকরণ করা হয় হিলিয়াম (Helium)।
অপর দিকে বিজ্ঞানী উইলিয়াম র্যামজি বায়ু ছাড়া ভিন্ন কোন উৎসে আর্গন সন্ধান অব্যাহত রাখলেন। ১৮৮৮ খ্রিষ্টাব্দে বিজ্ঞানী হিলেব্রাণ্ড (Hillebrand) ক্লিভাইট (clevite) নামক ইউরেনিয়াম আকরিককে লঘু সালফিউরিক এসিডে উত্তপ্ত করে আকরিকে অন্তর্ধৃত (occluded) একটি গ্যাসের অস্তিত্ব প্রমাণ করেণ। তিনি এই গ্যাসকে ভুলক্রমে নাইট্রোজেন জ্ঞান করেন; ফলে নতুন গ্যাস মৌল হিলিয়াম আবিষ্কারের গৌরব লাভে অসমর্থত হয়। র্যামজি হিলেব্রাণ্ডের প্রণালী অনুসারে ক্লিভাইটকে লঘু সালফিউরিক এসিড সহযোগে উত্তপ্ত ক'রে প্রাপ্ত গ্যাসে ২০% নাইট্রোজেনের অস্তিত্ব লাভ করেন। উপরন্তু কস্টিক অ্যালকালির উপর বিদ্যুৎ স্ফুলিঙ্গ প্রয়োগে নাইট্রোজেন বিদূরিত ক'রে বর্ণালী বিশ্লেষণেও D3-রেখা প্রাপ্ত হন। এটি ছিল জানসেন কর্তৃক গ্যাসীর সৌর আবরণে প্রাপ্ত D3-রেখা ব্যতীত আর কিছুই নয়। এবূপে প্রথম পার্থিব হিলিয়াম আবিষ্কৃত হয়। হিলিয়ামের ঘনত্ব, পারমাণবিক ভর ও এক পরমাণুকতা নির্ণীত হল। দেখা গেল এর ঘনত্ব ও পারমাণবিক ভর যথাক্রমে ১.৯৯ ও ৪। র্যামজি ও ট্রাভার্স (Travers) হিলিয়ামের ঘনত্ব পর্যবেক্ষণ করতে গিয়ে দেখেন যে বিভিন্ন আকরিক হতে প্রাপ্ত হিলিয়ামের ঘনত্ব বিভিন্ন। কাজেই তারা প্রাপ্ত গ্যাসকে ব্যাপন (diffusion) প্রণালীর সাহায্যে দুটি অংশে পৃথক করে তাদের ঘনত্বের মধ্যে উল্লেখযোগ্য রকম ব্যবধান পর্যবেক্ষণ করেন, এবং বর্ণালী বিশ্লেষণ করে অপেক্ষাকৃত ভারী অংশকে আর্গন ও হাল্কা অংশকে হিলিয়াম বলে নিরূপণ করেণ। এরূপে খনিজ পদার্থে আর্গনের অসিস্তত্ব আবিষ্কৃত হয়।
হিলিয়াম ও আর্গন আবিষ্কারের পর পর্যায় সারণিতে তাদের অবস্থান নির্বাচনে জটিলতা দেখা দেয়। ১৮৯৬ সালে জুলিও টমসন (Juliet Thomson) পর্যায় সূত্র প্রয়োগ করে পর্যায় সারণিতে একটি শূন্য-শ্রেণীর প্রস্তাব করেন এবং এতে ৪, ২০, ৩০, ৮৪, ১৩২, ও ২১২ পারমাণবিক গুরুত্বের ছয়টি মৌল থাকার সম্ভাবনা প্রকাশ করেন। তার এই প্রস্তাবনা র্যামজি ও ট্রাভার্সকে এই শূন্য শ্রেণীর অপরাপর মৌলের আবিষ্কারে উদ্বুদ্ধ করেন। হিলিয়ান ও আর্গন আবিষ্কৃত হওয়ায় তারা বায়ুতে আরও অনাবিষ্কৃত মৌলের অনুমান করেন ও তাদের অনুসন্ধানে ব্রতী হন।
১৮৯৮ খ্রিষ্টাব্দে র্যামজি ও ট্রার্ভাস তরল বায়ুর আংশিক পাতনে প্রাপ্ত তরল আর্গনের পুনঃ আংশিক পাতন করে অধিক উদ্বায়ী অংশ হতে একটি গ্যাস পৃথক করেন ও তার বণালী বিশ্লেষণ করে আর একটি নতুন গ্যাস নিয়ন (অর্থাৎ ‘নতুন’) আবিষ্কার করেন। এর ঘনত্ব ও আণবিক ভয় যথাক্রমে ১০.১ ও ২২.২ এবং এটিও এক-পরমাণুক। পরে তারা কম উদ্বায়ী অংশ হতে পৃথকভাবে দুটি নতুন নিষ্ক্রিয় গ্যাস যথা ক্রিপটন (অর্থাৎ গুপ্ত) ও জেনন (অর্থাৎ আগন্তুক) আবিষ্কার করেন।
এক কয়েক বছর পর ১৯০০ খ্রিষ্টাব্দে র্ডন (Dorn) রেডিয়ামের তেজস্ক্রিয় ক্ষয়জাত পদার্থ হতে সর্বশেষ নিষ্ক্রিয় গ্যাস রেডন আবিষ্কার করন। ৮৮/২২২ জধ ৮৬/২২২ জহ + ২/৪ ঐব ১৯০৩ খ্রিষ্টাব্দে র্যামজি ও সডি (Soddy) রেডিয়ামের তেজস্ক্রিয় বিভাজনের ফলে হিলিয়াম প্রাপ্ত হন এবং দেখা যায় অনেক তেজস্ক্রিয় মৌল হতেই হিলিয়াম বিচ্ছুরিত হয়।এইভাবে স্যার উইলিয়াম র্যামজি'র নিরলস, নিপুণ ও সুদীর্ঘ গবেষণার ফলে একটি শ্রেণীর সব কয়টি মৌলই একের পর এক আবিষ্কৃত হয়।[৩]
অবস্থান ও উৎস
সম্পাদনা- একমাত্র র্যাডন ব্যতীত সব ক'টি নিষ্ক্রীয় গ্যাসই বায়ুতে বর্তমান। তবে বায়ুতে এদের সর্বমোট পরিমাণ সর্ব্বোচ্চ ১.০% মাত্র। এজন্য এদেরকে বিরল গ্যাস (rare gases) নামেও অভিহিত করা হয়।
- খনিজ পদার্থঃ ইউরেনিনাইট (Uraninite), মোনাজাইট (Monazite) থোরিয়ানাইট (Thorianite), ক্লিভাইট (Cleveite), বেরিল (Beryl), কর্ডিরাইট (Cordierite), পিচ ব্লেণ্ড (Pitch blende) ইত্যাদি কিছু আকরিকে হিলিয়াম ও কিছু পরিমাণ আর্গন আবদ্ধ অবস্থায় থাকে। তাপপ্রয়োগে আকরিক থেকে গ্যাস বেরিয়ে আসে।
- প্রাকৃতিক গ্যাসঃ পেট্রোলিয়াম তৈলকূপ থেকে প্রাপ্ত প্রাকৃতিক গ্যাস (প্রধানত মিথেন) হিলিয়ামের একটি গুরুত্বপূর্ণ উৎস। এতে ০.৫ থেকে ১.৫ শতাংশ পর্যান্ত হিলিয়াম বিদ্যমান।
- সমুদ্র ও ঝর্ণার পানিঃ সমুদ্র পানিতে বায়ুমণ্ডলীয় গ্যাস দ্রবীভূত থাকে বিধায় এতে অল্প পরিমাণ নিষ্ক্রিয় গ্যাস পাওয়া যায়। কখনো কখনো ক্ষেত্রে ঝর্ণার পানিতে দ্রবীভূত অবস্থায় হিলিয়াম বিদ্যমান থাকে। যেমন Bourbon-lancy নামক ঝর্ণার খনিজ পানিতে ১.৮৪ শতাংশ পরিমাণে হিলিয়াম পাওয়া যায়। হিলিয়ামের একটি উল্লেখযোগ্য উৎস এই খনিজ পানি।
- রেডিয়ামের তেজস্ক্রিয় বিভাজন র্যাডন একটি তেজস্ক্রিয় (radioactive) মৌল। রেডিয়ামের তেজস্ক্রিয় ক্ষয়ের (radioactive decay) ফলে উৎপন্ন র্যাডন অনেক সময় বায়ুমণ্ডলে পাওয়া যায়।
| Abundance | Helium | Neon | Argon | Krypton | Xenon | Radon |
|---|---|---|---|---|---|---|
| Solar System (for each atom of silicon)[৪] | 2343 | 2.148 | 0.1025 | 5.515 × 10−5 | 5.391 × 10−6 | – |
| Earth's atmosphere (volume fraction in ppm)[৫] | 5.20 | 18.20 | 9340.00 | 1.10 | 0.09 | (0.06–18) × 10−19[৬] |
| Igneous rock (mass fraction in ppm)[৭] | 3 × 10−3 | 7 × 10−5 | 4 × 10−2 | – | – | 1.7 × 10−10 |
ইলেকট্রন বিন্যাস ও রাসায়নিক নিষ্ক্রিয়তা
সম্পাদনানিষ্ক্রিয় গ্যাসের ইলেকট্রন বিন্যাস পর্যবেক্ষণ করলে দেখা যায় যে, নিষ্ক্রিয় গ্যাসসমূহের সর্ববহিস্থ শক্তিস্তর অনুমোদিত সংখ্যক ইলেকট্রন দ্বারা পূর্ণ এবং ইলেকট্রনগুলো বিপরীতমুখী স্পিনসহ জোড়ায় জোড়ায় সজ্জিত। হিলিয়ামের বহিঃস্থ শক্তি স্তরে s অর্বিটালে দুটি, এবং অন্য সকল নিষ্ক্রিয় গ্যাসের সর্ববহিস্থ শক্তি স্তরে s ও p অর্বিটালে মোট চার জোড়ায় আটটি ইলেকট্রন আছে। বাইরের শক্তি স্তর ইলেকট্রন দ্বারা সম্পৃক্ত বলে এরা রাসায়নিকভাবে নিষ্ক্রিয়। পরমাণুর এরূপ ইলেকট্রন বিন্যাস খুবই সুস্থিত এবং রাসায়নিক ক্রিয়া বর্জিত। এদের আয়নীকরণ বিভবের উচ্চমানও এ সত্যকে পরিস্ফুট করে। ফলে এরা অপর কোন মৌলের সঙ্গে রাসায়নিক বিক্রিয়া দূরের কথা, এরা নিজেদের মধ্যেও বিক্রিয়া করে দ্বি-পরমাণুক অণু গঠন করতে পারে না।
নিম্নে এদের ইলেকট্রন বিন্যাস দেখান হল-
| মৌল | পারমাণবিক সংখ্যা | ইলেকট্রন বিন্যাস | যোজ্যতা ইলেকট্রন[৮] |
|---|---|---|---|
| He | ২ | 1s2 | 1s2 |
| Ne | ১০ | [He] 2s2 2p6 | 2s2 2p6 |
| Ar | ১৮ | [Ne] 3s2 3p6 | 3s2 3p6 |
| Kr | ৩৬ | [Ar] 3d10 4s2 4p6 | 4s2 4p6 |
| Xe | ৫৪ | [Kr] 4d10 5s2 5p6 | 5s2 5p6 |
| Rn | ৮৬ | [Xe] 4f14 5d10 6s2 6p6 | 6s2 6p6 |
ধর্ম
সম্পাদনাহিলিয়াম, নিয়ম, আর্গন, ক্রিপটন, জেনন ও র্যাডন-এরা সকলেই বর্ণহীন ও গন্ধহীন গ্যাস। এদের তরলীকরণ বেশ কষ্ট সাপেক্ষ। এরা পানিতে সামান্য পরিমাণে দ্রবণীয় ( ( 293 k-এ L-এ 8-40 mL)। পারমাণবিক ভর বৃদ্ধির সাথে পানিতে এদের দ্রাব্যতা বৃদ্ধি পায়।
নিষ্ক্রিয় গ্যাস পরমাণুসমূহের মধ্যে শুধুমাত্র ভৌত শক্তি (যেমন Van der Waals’ forces) থাকতে পারে বলে এদের স্ফুটনাঙ্ক ও গলনাঙ্ক অতিশয় কম। এদের মধ্যে তথা সমস্ত জ্ঞাত মৌলসমূহের মধ্যে হিলিয়ামের গলনাংক ও স্ফুটনাঙ্ক সবচেয়ে কম। গ্যাসসমূহের ক্ষেত্রে দেখা যায় তাদের গলনাংক ও স্ফুটনাঙ্ক তাদের পারমাণবিক ভর বৃদ্ধির সাথে বৃদ্ধি পায়।
অন্যান্য শ্রেণীর মৌলের তুলনার নিষ্ক্রিয় গ্যাস মৌলের আয়নীকরণ বিভব (ionisation potential) অনেক বেশি। পারমাণবিক ভর বৃন্ধির সাথে গ্যাস মৌলসমূহের আয়নীকরণ বিভব হ্রাস পায়। এদের ইলেকট্রন আসক্তি (electron affinity) শূন্যের কাছাকাছি। এরা সকলেই এক পরমাণুক। আপেক্ষিক তাপের অনুপাত Y=Cp/Cu=১.৬৭(স্থূলতা)।
নিচের ছকে এদের কযেকটি ভৌত ধর্ম সারণিবদ্ধ করা হলোঃ
রাসায়নিক ধর্ম
সম্পাদনা
প্রত্যেক নিষ্ক্রিয় গ্যাস পরমাণুর সর্ববহিস্থ শক্তি-স্তর ইলেকট্রন দ্বারা পূর্ণ (ns2np6) অর্থাৎ এদের পরমাণুর সর্ববহিস্থ স্তরে ৪টি করে (He-এর ক্ষেত্রে ২ টি) ইলেকট্রন আছে। এদের ব্যবহারে ইলেকট্রন দান (donate) বা গ্রহণ (accept ) করার কোনরূপ প্রবণতা দেখায় না বলে এরা আয়নীয় বা সমযোজী (covalent) যৌগ গঠন করতে পারে না। অতত্রব এরা সম্পূর্ণরূপে রাসায়নিক ক্রিয়াহীন। এতদ্সত্ত্বেও বিশেষ কোন কোন ক্ষেত্রে নিষ্ক্রিয় গ্যাস কর্তৃক বিভিন্ন যৌগ গঠনের প্রমাণ পাওয়া গেছে।
গুরুত্ব
সম্পাদনানিষ্ক্রিয় গ্যাসের গুরুত্ব অনেক। তত্ত্বীয় রসায়নে নিষ্ক্রিয় গ্যাসের আবিষ্কার বিশেষ গুরুত্বপূর্ণ ভূমিকা বহন করে। তত্ত্বীয় রসায়নের কোন দিক নেই যা নিষ্ক্রিয় গ্যাসের আবিষ্কারের ফলে প্রভাবান্বিত হয়নি। এদের অনেক অবদানের মধ্যে নিম্নের কয়েকটি প্রণিধানযোগ্য।
- পর্যায় সারণিতেঃ পর্যায় সারণিতে নিষ্ক্রিয় গ্যাসের অবস্থান তীব্র তড়িৎঋণাত্মক হ্যালোজেন মৌলসমূহের পরেই (১৭) অন্যদিকে, ১ম শ্রেণীর তীব্র ধনাত্মক ক্ষার ধাতু মৌলসমূহের আগে রয়েছে। অকস্মাৎ এই ধর্ম পরিবর্তনের মধ্যে একটা বিরাট অসামঞ্জস্যতা দৃষ্ট হয়। নিষ্ক্রিয় গ্যাস মৌলসমূহের আবিষ্কারের ফলে তাদেরকে শূন্য (০) শ্রেণীতে (মেন্ডেলিফ অনুযায়ী) স্থাপন করায় এই দুই বিপরীতধর্মী মৌল শ্রেণীর মধ্যে সেতুবন্ধ রচিত হয়েছে এবং অসামঞ্জস্যতা ঘুচে সমন্বয় ঘটেছে।
- পারমাণবিক গঠনেঃ একমাত্র হিলিয়াম ব্যতীত সব নিষ্ক্রিয় গ্যাস পরমাণুর শেষ কক্ষে আটটি (৮ করে ইলেকট্রন আছে। হিলিয়ামের ক্ষেত্রে এই ইলেকট্রন সংখ্যা ২টি। এতে বোর ও বুরি (Bury) এই তত্ত্ব প্রকাশে সক্ষম হন যে পরমাণুর সর্ববহিঃস্থ স্তর ৮টির অধিক ইলেকট্রন ধারণ করতে পারে না।
- যোজ্যতার ইলেকট্রিনীয় তত্ত্ব : নিষ্ক্রিয় গ্যাসের ইলেকট্রন বিন্যাস পর্যবেক্ষণ করত: লুই (Lewis) ও কোসেল (Kossel) পরমাণুতে ইলেকট্রনের ভারসাম্যমূলক বিন্যাস ধারণা (stable configuration concept) প্রস্তাব করেন। তাদের প্রত্যেক মৌলই তার পরমাণুর সর্ববহিরিস্থ স্তরে ইলেকট্রন স্থানান্তর (আয়নীয় বন্ধন) বা শেয়ার (সমযোজী বন্ধন) করে তার নিকটতম নিষ্ক্রিয় গ্যাসের ইলেকট্রন-বিন্যাস অর্জন করে। অতএব, একটি মৌল তার নিকটতম নিষ্ক্রিয় গ্যাস মৌলের ইলেকট্রনীয় গঠন অর্জন কল্পে যত সংখ্যক ইলেকট্রন দান, গ্রহণ বা ভাগাভাগি করে থাকে তাকে মৌলটির যোজ্যতা বলে।
- তেজস্ক্রিয়তায়ঃ তেজস্ক্রিয় মৌল হতে α-কণা বিচ্ছুরিত হয়। এটা ধনাত্মক দ্বি-আধান যুক্ত হিলিয়াম পরমাণু (4He2+)। এই তথ্য তেজস্ক্রিয় বিভাজন তত্ত্ব ও শ্রেণী অপসারণ সূত্র (group displacement law) সংবচনায় সাহায্য করে।
- আইসোটোপ আবিষ্কারঃ অতেজস্ক্রিয় মৌলসমূহের মধ্যে নিয়নের আইসোটোপ সর্বপ্রথম পৃথক করা হয়। এতে অপরাপর অতেজস্ক্রিয় মৌলের আইসোটোপ পৃথকীকরণের প্রচেষ্টা চলে।
ব্যবহার
সম্পাদনাবিভিন্ন নিষ্ক্রিয় গ্যাসের ব্যবহার নিম্নে বর্ণনা করা হলোঃ
হিলিয়াম
সম্পাদনা(১) বেলুন ও আকাশ যানে হিলিয়াম ব্যবহৃত হয়। এটি হাইড্রোজেন অপেক্ষা ভারী হলেও এর উত্তোলন ক্ষমতা হাইড্রোজেনের প্রায় কাছাকাছি (৯২%) অথচ এটি অদাহ্য ও অপেক্ষাকৃত কম ব্যাপনীয় (less diffusible)। এজন্য এ কাজে হাইড্রোজেন অপেক্ষা হিলিয়াম অধিক উপযোগী।[৯]
(২) রক্তে হিলিয়াম অপেক্ষা নাইট্রোজেন অধিকতর দ্রবণীয়। এই জন্য ডুবুরী যন্ত্রে বায়ুর পরিবর্তে অক্সিজেনের সাথে মিশ্রিত অবস্থায় হিলিয়াম (২০% ঙ২ ও ৮০% ঐব) ব্যবহৃত হয়। এতে সমুদ্রের তলদেশে উচ্চ চাপে বায়ুতে শ্বাস-প্রশ্বাসের যে অসুবিধা হয় তা দূরীভূত হয়। কারণ উচ্চ চাপে বায়ুতে নাইট্রোজেন রক্তে দ্রবীভূত হয়ে যায় আর পানির উপরে উঠা মাত্রই চাপ কমে যায়, ফলে দ্রবীভূত নাইট্রোজেন বের হয়ে আসে এবং রক্তের মধ্যে বুদদ সৃষ্টি করে। এতে অকস্মাৎ ব্যথা সৃষ্টি হয়। হিলিয়াম যুক্ত অক্সিজেন ব্যবহারে এই অসুবিধা হয় না।[১০]
(৩) হাঁপানী প্রভৃতি রোগে শ্বাসকার্যের সহায়তার জন্য হিলিয়াম মিশ্রিত অক্সিজেন ব্যবহৃত হয়।
(৪) নিম্ন তাপমাত্রার গবেষণাকার্যে তরল হিলিয়াম (৪.১ K) ব্যবহৃত হয়।
(৫) নিম্ন তাপমাত্রা পরিমাপে ব্যবহৃত গ্যাস থার্মোমিটারে হিলিয়াম ব্যবহৃত হয়।
(৬) সহজেই জারিত হয় এমন ধাতু ও ধাতু সংকরের গলন এবং জোড়া লাগানোর সময় নিষ্ক্রিয় পরিবেশ সৃষ্টি করতে হিলিয়াম ব্যবহৃত হয়।
(৭) বায়ু অপেক্ষা হিলিয়াম হালকা বলে এটি বৃহদাকার আকাশ যানের টায়ারে ব্যবহৃত হয়।[১১]
(৮) এর সান্দ্রতা (viscosity ) একটু অধিক বলে কম্পাস ও নাবিকদের অন্যান্য যন্ত্রে এটি ড্যাম্পার (damper) হিসেবে ব্যবহৃত হয়।
(৯) এটি বৈদ্যুতিক ট্রান্সফরমার, টিউব লাইট ও রেডিও টিউবে ব্যবহৃত হয়।
(১০) মাটির নিচে পেট্রোলিয়াম স্থানান্তর নির্দেশনায় ট্রেসার (tracer) গ্যাস হিসেবে এটি ব্যবহৃত হয়।
নিয়ন
সম্পাদনা(১) নিয়ন প্রধানত আলোক উৎপাদন ও আলোকসজ্জায় ব্যবহৃত হয়। নিয়ন-টিউবে এটি অত্যুজ্জ্বল লাল আলো উৎপাদন করে। এটি পারদ (মারকারি) বাষ্পের সাথে মিশ্রিত থাকলে সবুজ বা নীল আলো পাওয়া যায়। নিয়ন গ্যাস বা তার বিভিন্ন মিশ্রণের সাথে বিভিন্ন বর্ণের কাচ ব্যবহার করে আলোর বৈচিত সৃষ্টি করা সম্ভব। নিয়ন আলো কুয়াসার মধ্যেও দেখা যায় -এই জন্য বৈমানিকগণ আলোক-সংকেতরূপে এই আলো ব্যবহার করে থাকেন।
(২) নিয়নের সাহায্যে প্রতিপ্রভ নলে আলোর বৈচিত্র্য সৃষ্টি করে ব্যবসায় ক্ষেত্রে রকমারি বিজ্ঞাপনে নিয়ন যথেষ্ট পরিমাণে ব্যবহৃত হয়।
(৩) কোন নিদিষ্ট বিভব সীমা (voltage limit) অতিক্রান্ত না হওয়া পর্যন্ত নিয়ন-হিলিয়াম মিশ্রণ বিদ্যুৎ পরিবহন করে না। এই মাত্রা অর্থাৎ উচ্চ বিভব প্রয়োগ হলে এটি বিদ্যুৎ পরিবাহী। কাজেই ভোল্টমিটার ও রেকটিফায়ার প্রভৃতি যন্ত্রের সংরক্ষণে এই মিশ্রণ ব্যবহৃত হয়।
আর্গন
সম্পাদনা(১) আর্গন প্রধানত ইলেকট্রিক বাল্ব পূরণে ব্যবহৃত হয়। বাল্বে আর্গন থাকার দরুন টাংস্টেন সূত্র (tungsten filament) সহজে বাষ্পীভূত হয় না ফলে বালবের পরমায়ু অনেকাংশে বর্ধিত হয়।
(২) রেডিও-এর বাল্ব ও রেকটিফায়ার-এ আর্গন ব্যবহৃত হয়।
(৩) ঝালাই-এর কাজে নিষ্ক্রিয় পরিবেশ সৃষ্টি করতে আর্গন ব্যবহৃত হয়।
(৪) গ্যাস ক্লোমাটোগ্রাফীতেও এর ব্যবহার আছে।
ক্রিপ্টন
সম্পাদনা(১) আর্গনের মত ক্রিপটনও টিউব বাতিতে ব্যবহৃত হয়।
(২) কসমিক রশ্মি পরিমাপে আয়নীকরণ প্রকোষ্ঠে (Ionisation chamber) ক্রিপটন ব্যবহৃত হয়।
(৩) ক্রিপটন পারমাণবিক দীপ (Krypton atomic lamp) নির্মাণে Kr 85-এর ব্যবহার আছে।
(৪) খনি-শ্রমিকদের ‘ক্যাপ-ল্যাম্পে’ ক্রিপটন ব্যবহার করা হয়।
জেনন
সম্পাদনা(১) দ্রুত গতিসম্পন্ন ফ্লাশ-লাইটে জেনন আছে।
(২) নিউট্রন Y-রশ্মি ও নিরপেক্ষ মেসন (meson) কণা শনাক্তকরণে বুদবুদ প্রকোষ্ঠ (Bubble chamber) তৈরি করতে এটি ব্যবহৃত হয়।
রেডন
সম্পাদনা(১) রেডিও-থ্যারাপি চিকিৎসায় শরীরে ক্ষতিকর বৃদ্ধি নাশে এটি ব্যবহৃত হয়।
(২) ক্যানসারের মত দুরারোগ্য ব্যাধি নিরসনেও রেডন ব্যবহৃত হয়।
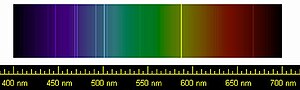
বর্ণ বিচ্ছুরণ
সম্পাদনা |  |  |  |  |
 |  |  |  |  |
 |  |  |  |  |
 |  |  |  |  |
| হিলিয়াম | নিয়ন | আর্গন (ছবিতে কিছুটা মার্কারির সাথে আর্গন) | ক্রিপ্টন | জেনন |
তথ্যসূত্র
সম্পাদনা- ↑ আইইউপ্যাক অনুসারে মাঝে মাঝে শূন্যতম শ্রেণীও বলা হয়)
- ↑ নোবল গ্যাসসমূহ
- ↑ রসায়নের ইতিহাস - নোবল গ্যাসসমূহ
- ↑ Lodders, Katharina (২০০৩)। "Solar System Abundances and Condensation Temperatures of the Elements"। The Astrophysical Journal। 591 (2): 1220–1247। ডিওআই:10.1086/375492। বিবকোড:2003ApJ...591.1220L।
- ↑ "The Atmosphere"। National Weather Service। সংগ্রহের তারিখ ২০০৮-০৬-০১।
- ↑ Häussinger, Peter; Glatthaar, Reinhard; Rhode, Wilhelm; Kick, Helmut; Benkmann, Christian; Weber, Josef; Wunschel, Hans-Jörg; Stenke, Viktor; Leicht, Edith; Stenger, Hermann (২০০২)। "Noble gases"। Ullmann's Encyclopedia of Industrial Chemistry। Wiley। ডিওআই:10.1002/14356007.a17_485।
- ↑ Greenwood 1997, পৃ. 891
- ↑ গ্রুপ ১৮ নোবল গ্যাসসমূহ
- ↑ Freudenrich, Craig (২০০৮)। "How Blimps Work"। HowStuffWorks। সংগ্রহের তারিখ ৩ জুলাই ২০০৮।
- ↑ Fowler, B.; Ackles, K. N.; Porlier, G. (১৯৮৫)। "Effects of inert gas narcosis on behavior—a critical review"। Undersea Biomed. Res.। 12 (4): 369–402। আইএসএসএন 0093-5387। ওসিএলসি 2068005। পিএমআইডি 4082343। Archived from the original on ২৫ ডিসেম্বর ২০১০। সংগ্রহের তারিখ ৮ এপ্রিল ২০০৮।
- ↑ Freudenrich, Craig (২০০৮)। "How Blimps Work"। HowStuffWorks। সংগ্রহের তারিখ ৩ জুলাই ২০০৮।




