نافلزها
نافلزها گروهی از عناصر شیمیایی هستند. در جدول تناوبی عناصر فلز، نافلز یا شبه فلز هستند.
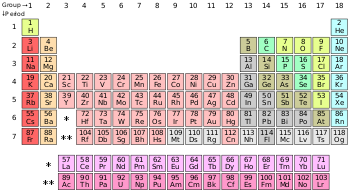
غیر از هیدروژن، بقیه نافلزات در منطقه بلوک پی قرار گرفتهاند. هلیوم، اگر چه یک عنصر متعلق به بلوک اس است، اما بهطور معمول در بالای نئون و در بلوک پی قرار میگیرد، علت آن هم دارا بودن خاصیت گاز نجیب است.
نافلزات عبارتند از:
خصوصیات اصلی
ویرایش- • در مقایسه با فلزات، عموماً رسانندهٔ گرما و الکتریسیته نیستند البته برخی از آنها مانند کربن و الماس میتوانند به دلیل ساختار بلوری خاص خود به ترتیب جریان الکتریسیته و گرما را از خود عبور دهند.
- • اکسید آنها خواص اسیدی نشان میدهد، درحالیکه اکسید فلزات خاصیت بازی دارد.
- • در شکل جامد آنها مات و شکننده هستند، جلای فلزی ندارند، شمش پذیر نیستند و خاصیت چکش خواری ندارند.
- • معمولاً جرم حجمی یا چگالی پایینتری نسبت به فلزات دارند.
- • بهطور قابل توجهی دمای ذوب و جوش پایینتری نسبت به فلزات دارند.
- • نافلزات خاصیت تمایل الکترونگیری (الکترونگاتیویته) بالاتری دارند.
- • حالت عمومی آنها گازی میباشد که البته برم نافلزی مایع و گوگرد، فسفر، ید، سلنیم و کربن حالت جامد دارند.
- • در واکنشهای شیمیایی تمایل به گرفتن الکترون و تشکیل آنیون ویا به اشتراک گذاشتن الکترون را دارند.
تقسیمبندی نافلزات
ویرایشاین عناصر از نظر تعداد اتم در مولکولهایشان به سه دسته نافلزات چند اتمی، نافلزات دو اتمی و و گازهای نجیب تقسیم میشوند.
نافلزات چند اتمی
ویرایشاین نافلزات شامل عناصر کربن و سلنیم و گوگرد و فسفر است.

تمامی این نافلزات در دمای اتاق به حالت جامدند. این عناصر مولکولهایی بیش از دواتم تشکیل میدهند. کربن میتواند جامدهای کووالانسی غول آسایی مانند گرافیت و الماس بسازد. این عناصر نسبت به گروه بالا رسانای بهتری برای برق اند مثلاً گرافیت یک ماده نیمه رساناست. این گروه نسبت به گروه اول عدد الکترونگاتیوی کمتری دارند و بنا راین بیشتر تمایل دارند تا الکترونهای خود را به اشتراک بگذارند و پیوند کووالانسی تشکیل دهند اگر چه عدد الکترونگاتیوی آنها نسبت به فلزات بسیار بیشتر است. این گروه در ایجاد چرخه حیات بسیار نقش مهمی دارند و کربن ماده اصلی سازنده مولکولهای زیستی است. این گروه دمای ذوب و جوش بسیار بالاتری نسبت به گروه دوم دارند.
نافلزات دواتمی
ویرایش
این نافلزات شامل نه عنصر یعنی تمامی هالوژنها و عناصر دو اتمی اکسیژن و نیتروژن و هیدروژن است.این عناصر رسانای بسیار ضعیف برق اند ولی بسیار الکترونگاتیو بوده و در ترکیبات یونی پیوندهای محکمی تشکیل میدهند. نکته دیگر این است که از میان این عناصر برم به حالت مایع و ید به حالت جامد در دمای اتاقند.
نافلزهای واکنش پذیر
ویرایشدسته ای متنوع از نافلزات در جدول هستند که شامل عناصر کربن، نیتروژن، فسفر، اکسیژن، گوگرد، سلنیم، فلوئور، کلر، برم و ید میباشد. این عناصر از راست به گازهای نجیب و از چپ به شبه فلزات محدود میشوند.از نظر فیزیکی ۵ عضو این گروه جامد، یک عضو آن مایع (برم) و ۵ عضو دیگر گازی هستند در نتیجه از این منظر این گروه تنها گروهی است که در دمای اتاق هر سه حالت فیزیکی ماده را شامل میشود.
گازهای نجیب
ویرایش
گاز نجیب (گازهای کمیاب یا گازهای بیاثر) که بیبو و بیرنگ هستند، به عنصرهای هلیوم، نئون، آرگون، کریپتون، گزنون، رادون و آناناکتیوم گفته میشود که همه در دمای اتاق گازی هستند و در گروه A8 جدول مندلیف قرار دارند. به استثنای هلیوم، تمام گازهای نجیب دارای آرایش الکترونی خارجی ns2 np6 هستند که آرایشهای بسیار پایدارند.
تمامی این گازها تک اتمی هستند و به مقدار کم در اتمسفر یافت میشوند. (تنها حدود یک درصد حجم هوا را تشکیل میدهند). در بین گازهای بیاثر، رادون عنصری رادیواکتیو و خطرناک است. گازهای بیاثر بیشترین انرژی یونیزاسیون را داشته و الکترونگاتیویته آنها بسیار کم و ناچیز است. این گازها نقطه ذوب پایینی دارند (هلیوم کمترین مقدار نقطه ذوب را دارد) و همگی در هوای اتاق به شکل گاز هستند.
منابع
ویرایش- ویکیپدیای انگلیسی
- Wiberg N 2001, Inorganic chemistry, Academic Press, San Diego, ISBN 0-12-352651-5

