קבוצה פונקציונלית
בכימיה, קבוצה פונקציונלית (אנגלית: Functional group) היא קבוצת אטומים בתרכובת, המשפיעה באופן מכריע על התנהגותה הפיזיקלית והכימית. המונח מתייחס בדרך כלל לקבוצות כימיות של תרכובות אורגניות.
הגדרתן של קבוצות פונקציונליות (שהן למעשה תבניות ייחודיות) מאפשרת לסווג תרכובות כימיות למשפחות שלהן תכונות כימיות ופיזיקליות דומות.
מונחון IUPAC מסדיר את אופן מתן השמות לתרכובות הפחמן לפי הקבוצה הפונקציונלית שלהן.
התכונות הנקבעות על ידי הקבוצות הפונקציונליות
עריכהקישור בין מולקולרי
עריכה- קשרי מימן במולקולות המכילות חנקן, חמצן או פלואור כאטומים צמודים למימן;
- קשרי ואן דר ואלס במולקולות שאינן מכילות את היסודות חנקן, חמצן או פלואור כאטומים צמודים למימן.
- כל המולקולות הנזכרות בסעיף הקודם יכולות לקיים קשרי מימן בקצה של הקבוצות הפונקציונליות הנ"ל ובמקביל לקיים גם קשרי ואן דר ואלס באמצעות השרשרת הפחמנית שלהן.
- קבוצות שיכולות לקיים אך ורק קשרי ואן דר ואלס הן:
- CHX (ההלוגנים Cl, Br, I) שמאפיינים אלקילהלידים. (X=הלוגן כלשהו).
- (אלדהידים). יש להבחין בין קבוצת OH המאפיינת כהלים שבה קבוצת OH מקיימת קשר קוולנטי יחיד עם השלב הפחמני לעומת קבוצת CHO (אלדהיד) שבה מקיים אטום הפחמן קשר יחיד עם המימן וקשר כפול עם החמצן.
- COC (אתר). אטום החמצן נמצא בין הפחמנים כאשר הוא חולק קשר יחיד עם כל אחד מהם ולכן אינו מקיים קשרי מימן.
- CONa - מתכות אלקליות מטור ראשון במערכה המחזורית המקיימות תגובה עם כהלים שבמהלכה נפלט המימן (במצב צבירה גז) מקבוצת OH של הכהל, היסוד האלקלי יוצר עם התרכובת האורגאנית חומר יוני באמצעות החמצן הנותר מקבוצת OH.
רמת החומציות
עריכה- חומרים נטרליים שאינם מתפרקים לחומצה או בסיס;
- אלקאנים (פחמימנים בעלי שלד פחמימני בלבד וקשרים יחידים).
- אלקנים (פחמימנים בעלי שלד פחמני בלבד וקשרים כפולים).
- אלקילהלידים (בעלי קבוצת CHX).
- חומצות אורגניות בעלות קבוצה COOH. הפחמן של קבוצה זו מקיים קשר יחיד עם הפחמן שלפניו בשרשרת הפחמנית, קשר כפול עם חמצן אחד וקשר יחיד עם קבוצת OH. בשל האלקטרושליליות הגבוהה של שני הפחמנים, משתחרר המימן למים והופך אותם מH2O לH3O+ (יוני הידרוניום).
- בסיסים אורגנים בעלי קבוצת NH.
מסיסות
עריכה- שרשראות פחמימניות בעלות קבוצה פונקציונלית המקיימת קשרי מימן מסיסות גם במים (בשל קשרי המימן של המים) וגם בנוזלים וגזים אחרים (בשל קשרי ואן דר ואלס של השרשרת הפחמימנית עצמה).
- הערה: מידת המסיסות במים תיקבע על ידי אורך השרשרת הפחמימנית ומספר ההסתעפויות שלה. ככל שהשרשרת גדולה יותר ופחות מסועפת, כך גדל שטח המגע בין מולקולות החומר האורגאני ובמקרים מסוימים המולקולה כל-כך גדולה עד שמסיסותה במים זניחה למרות היותה בעלת קבוצה פונציונלית המקיימת קשרי מימן.
- שרשראות פחמימניות בעלות קבוצה פונקציונלית שאינה מקיימת קשרי מימן אלא רק קשרי ואן דר ואלס, אינן מסיסות במים אך מסיסות במגוון נוזלים וגזים אחרים.
- הערה: קבוצה יוצאת דופן היא CONa שאינה יוצרת קשרי מימן אך משום שהיא יוצרת חומר יוני מקוטב, המולקולה מסיסה במים.
קבוצות פונקציונליות חשובות
עריכהפחמימנים
עריכה| קבוצה | נוסחת מבנה | מבנה לואיס |
|---|---|---|
| אלקאן | R(CH2)nH |  |
| אלקן | R2C=CR2 | 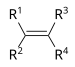 |
| אלקין | RC≡CR' |  |
| הלואלקאן | R-X |  |
| בנזיל | RC6H5 RPh | 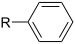 |
קבוצות המכילות חמצן
עריכה| קבוצה | נוסחת מבנה | מבנה לואיס |
|---|---|---|
| הידרוקסיל (כוהל) | ROH |  |
| קטון | RCOR' |  |
| אלדהיד | RCHO |  |
| אציל | RCOX |  |
| קרבונט | ROCOOR' | 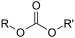 |
| קרבוקסיל (חומצה קרבוקסילית) | RCOOH |  |
| קרבוקסילט | RCOO− |  |
| אסטר | RCOOR' |  |
| הידרופראוקסיד | ROOH |  |
| פראוקסיד | ROOR' |  |
| אתר | ROR' | 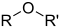 |
| המיאצטל | RCH(OR')(OH) |  |
| המיקטאל | RC(ORʺ)(OH)R' |  |
| אצטל | RCH(OR')(OR") |  |
קבוצות המכילות חנקן
עריכה| קבוצה ראשית | נוסחת מבנה | מבנה לואיס | |
|---|---|---|---|
| אמיד | RCONR2 |  | |
| קרבאמאט | ROCONR2 |  | |
| אמין | אמין ראשוני | RNH2 |  |
| אמין שניוני | R2NH | 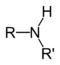 | |
| אמין שלישוני | R3N |  | |
| אמין רבעוני | R4N+ |  | |
| אימין | קטאימין ראשוני | RC(=NH)R' | 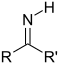 |
| קטאימין שניוני |  |  | |
| אלדאימין ראשוני | RC(=NH)H |  | |
| אלדאימין שניוני | RC(=NR')H |  | |
| אימיד | (RCO)2NR' | 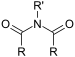 | |
| אזיד | RN3 |  | |
| אזו | RN2R' | 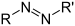 | |
| ציאנט | ציאנט | ROCN | 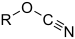 |
| איזוציאנט | RNCO |  | |
| ניטראט | RONO2 |  | |
| ניטריל | ניטריל | RCN |  |
| איזוניטריל | RNC |  | |
| ניטריט | ניטרוסואוקסי | RONO | 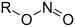 |
| ניטרו | RNO2 |  | |
| ניטרוסו | RNO |  | |
| אוקסים | RCH=NOH | 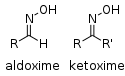 | |
| נגזרות פרידין | פרידיל | RC5H4N | |
קבוצות המכילות גופרית
עריכה| קבוצה | נוסחת מבנה | מבנה לואיס | |
|---|---|---|---|
| תיול | RSH |  | |
| סולפיד (תיואתר) | RSR' |  | |
| דיסולפיד | RSSR' | 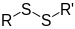 | |
| סולפוקסיד | RSOR' |  | |
| סולפון | RSO2R' |  | |
| חומצה סולפינית | RSO2H |  | |
| חומצה סולפונית | RSO3H |  | |
| תיוציאנט | תיוציאנט | RSCN |  |
| איזותיוציאנט | RNCS | 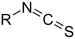 | |
| תיוקטון | RCSR' |  | |
| תיאל | RCSH |  | |
| תיואסטר | RSOSR |  | |
| סולפונאמיד | RSO2NR2 |  | |
קבוצות המכילות זרחן
עריכה| קבוצה | נוסחת מבנה | מבנה לואיס |
|---|---|---|
| פוספין | R3P | 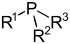 |
| חומצה פוספונית |  |  |
| פוספאט |  |  |
| פוספודיאסטר | HOPO(OR)2 |  |
ראו גם
עריכהקישורים חיצוניים
עריכה- קבוצה פונקציונלית, באתר אנציקלופדיה בריטניקה (באנגלית)
🔥 Top keywords: עמוד ראשימיוחד:חיפושחג הקורבןדור הררירוקדים עם כוכבים (עונה 3, קשת)לירז צ'רכיקדחת מערב הנילוסאילניתמלחמת חרבות ברזליורו 2024מיוחד:שינויים אחרוניםאליהו רביבותום אבניעמוס הוכשטייןרוקדים עם כוכבים (קשת)דנית גרינברגבלקספייסבלתי הפיך (ספר)עופר ינאיפרשת משחקי חברהמריאנו אידלמןאליפות אירופה בכדורגלהפועל תל אביב (כדורסל)לוסי איובנחמן שיקיליאן אמבפההקול בראש 2גאולה אבן-סעריוליה שמאלוב-ברקוביץ'בית הדרקוןשמעון מזרחיליגת העל בכדורסלהדירוג העולמי של פיפ"אאף אחד לא עוזב את פאלו אלטוישראלאנה ארונובדרגות צה"ליום האבברידג'רטון


